
1. Atom digambarkan sebagai bola pejal yang sangat kecil.
2. Atom merupakan terkecil yang tidak dapat dipecah lagi.
3. Atom dari unsur yang sama memiliki sifat sama, sedangkan atom dari unsur yang berbeda memiliki massa dan sifat yang berbeda.
4. Senyawa terbentuk jika atom bergabung satu sama lain.
5. Reaksi kimia hanya melibatkan penataan ulang atom-atom sehingga tidak ada atom yang berubah akibat reaksi kimia.Kelemahannya: ternyata atom masih bisa dipecah lagi.
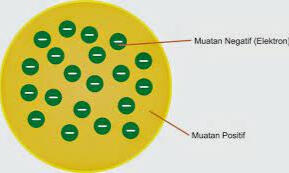
Thomson mengemukakan bahwa atom tersusun dari elektron-elektron yang tersebar secara merata dalam bola bermuatan positif, keadaan ini mirip dengan roti kismis, dengan elektron sebagai iklan yang tersebar di seluruh bagian roti.Kelemahannya: tidak menyatakan gerakan elektron dan atom.
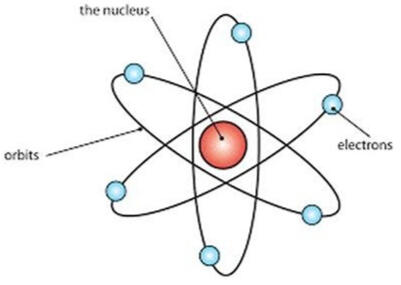
Menurut Rutherford, atom terdiri atas inti yang bermuatan positif yang berada di pusat atom serta elektron yang bergerak mengelilingi inti, seperti halnya planet-planet mengelilingi matahari.Kelemahannya: tidak dapat dijelaskan akibat mengapa elektron tidak jatuh ke inti atom gaya elektrostatis inti terhadap elektron.

Menurut Niels Bohr:
1. Atom terdiri atas inti yang bermuatan positif dan elektron-elektron yang bermuatan negatif yang beredar di sekitar inti.
2. Dalam atom, elektron yang beredar mengelilingi inti atom pada orbit tertentu yang dikenal sebagai lintasan stasioner yang selanjutnya disebut dengan tingkat energi utama (kulit atom).
3. Selama elektron berada dalam lintasan stasioner, energi akan tetap, sehingga tidak ada energi yang dipancarkan maupun diserap.
4. Elektron dapat berpindah dari lintasan stasioner yang lebih rendah ke lintasan stasioner yang lebih tinggi jika menyerap energi, dan sebaliknya.Kelemahannya : hanya dapat dijelaskan spektrum dari atom atau ion yang mengandung satu elektron. Jadi model atom Bohr tidak sesuai dengan spektrum atom atau ion yang berelektron banyak.

1. Menurut Louis Victor de Broglie elektron dalam atom dapat dilihat sebagai partikel gelombang
2. Menurut Werner Heisenberg letak dan kedudukan elektron dalam atom tidak dapat dipastikan yang ada hanya kebolehjadian menemukan elektron yang disebut orbital.
3. Menurut Erwin Schrodinger gambaran gerak elektron dalam atom berupa gelombang.